Uno de los objetivos más buscados en ciencia es generar conocimiento para curar el cáncer. Para eso, se investiga sin cuartel. Científicos de la Universidad Nacional de La Plata estudian desde hace más de tres décadas los efectos de diversos agentes mutagénicos sobre los cromosomas de células animales y humanas, que se utilizan para el tratamiento contra el cáncer.
Los investigadores pertenecen al Instituto Multidisciplinario de Biología Celular (IMBICE), perteneciente a las Facultades de Ciencias Exactas y Ciencias Naturales y Museo de la UNLP, al CONICET y a la CICPBA.
Los cromosomas son estructuras formadas por ADN y proteínas, que se encuentran en el núcleo de las células y que contienen a los genes. Las partes funcionales principales de los cromosomas son las constricciones primarias o centrómeros y los extremos o telómeros. La citogenética es el estudio de los cromosomas y sus anomalías (numéricas y estructurales, ya sean espontáneas o inducidas), mientras que la mutagénesis (= generación de mutaciones) es el estudio de los cambios genéticos o mutaciones inducidas por diversos agentes, ya sea de naturaleza física (radiaciones), química (alcohol, tabaco, compuestos antitumorales y otros) o biológica (virus).
Las aberraciones cromosómicas pueden ser numéricas (como la poliploidía o la aneuploidía, que implican, respectivamente, la presencia de tres o más juegos completos de cromosomas o de uno o unos pocos cromosomas extras o ausentes respecto del contenido normal de cromosomas de la célula en cuestión) o estructurales (como, por ejemplo, un cromosoma en forma de anillo o un cromosoma dicéntrico, es decir, con dos centrómeros). Uno de los campos de estudio más importantes dentro de la citogenética es el dedicado a las aberraciones o anomalías cromosómicas inducidas por agentes mutagénicos (es decir, que generan daño genético, ya sea a nivel citogenético (cromosomas) o molecular (ADN). Cuando el agente causa la rotura de los cromosomas, se denomina clastogénico.
La importancia de estudiar el daño inducido por un agente clastogénico radica en que la generación de daño estructural a nivel cromosómico puede ocasionar la muerte de la célula afectada o llevar al desarrollo de células tumorales (con replicación descontrolada). Asimismo, si el daño cromosómico afecta a las células de la línea germinal, entonces el daño puede transmitirse a la descendencia de los progenitores en cuestión si las gametas que intervienen en la formación del cigoto (óvulo fecundado, que luego se transforma en embrión), resultan afectadas. Por ello, el estudio del daño cromosómico inducido por diversos agentes mutagénicos, resulta de gran interés para la salud humana. Dichos estudios comprenden tanto a individuos laboral o accidentalmente expuestos a radiaciones u otros mutágenos, como a aquellos que, por razones médicas, son sometidos a una radio- o quimioterapia.
El Laboratorio de Citogenética y Mutagénesis (LCyM) del IMBICE, tiene como línea principal de investigación, el estudio del daño cromosómico inducido por compuestos antitumorales en células animales y humanas y está a cargo del Dr. Alejandro Bolzán (investigador del CONICET y Jefe del laboratorio desde el año 2006), junto con su becaria doctoral Andrea Cardozo (también del CONICET, realizando su tesis doctoral en la Facultad de Ciencias Exactas de la UNLP).
“El objetivo general de esta línea de investigación es analizar la inestabilidad a nivel cromosómica, ya sea espontánea o inducida por diversos mutágenos, presente en células animales y humanas y los mecanismos subyacentes a dicha inestabilidad. Mediante diversas metodologías de citogenética clásica (tinción con Giemsa, intercambios de cromátidas hermanas, etc.) y molecular (Hibridación In Situ Fluorescente o FISH), buscamos determinar los efectos de diversos compuestos antitumorales, es decir, que se utilizan en terapias contra el cáncer (quimioterapias) sobre los cromosomas de células humanas y animales, en particular sus telómeros”, detalló el Dr. Bolzán.
Esto es debido a que, en las últimas décadas, el estudio de los telómeros o extremos cromosómicos de las células eucariotas ha adquirido una gran importancia, dado el rol fundamental que los mismos cumplen en el mantenimiento de la estabilidad del genoma, el envejecimiento y el cáncer. En particular, actualmente se están estudiando en el LCyM los efectos de los antibióticos antitumorales bleomicina (que es radiomimético, es decir, tiene una acción mutagénica parecida a la de las radiaciones ionizantes) y estreptozotocina (que además es diabetogénico, es decir, induce diabetes) sobre los telómeros de células humanas (las cuales son obtenidas directamente del banco de células del IMBICE).
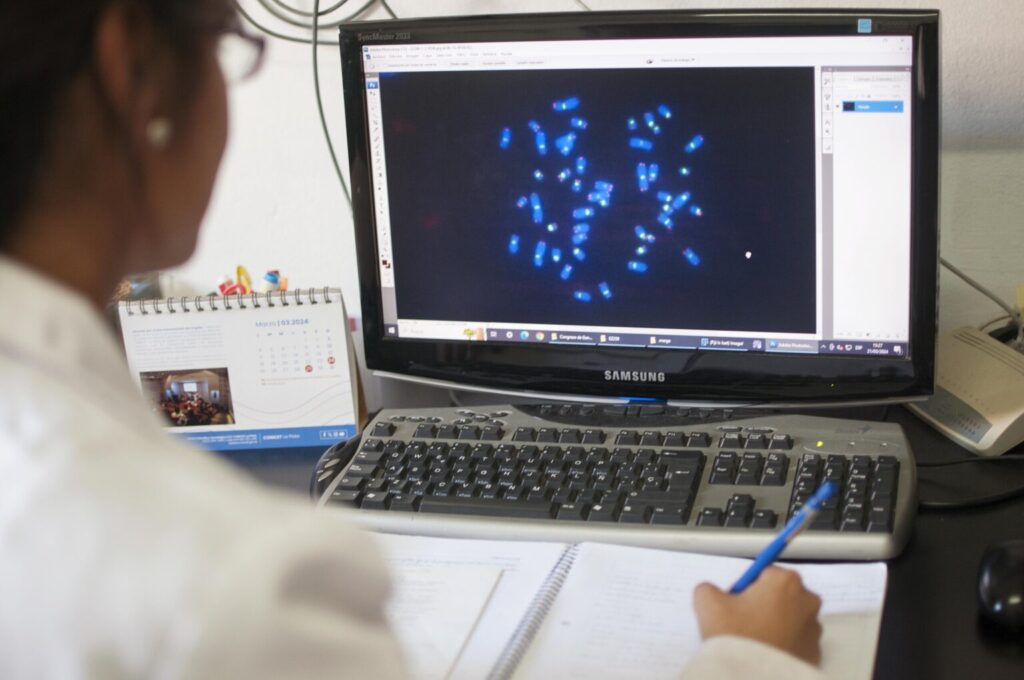
Estos estudios se llevan a cabo utilizando la técnica de FISH con sondas (secuencias de ADN, marcadas con un colorante fluorescente o fluorocromo específico) que marcan regiones específicas de los cromosomas (sus constricciones primarias o centrómeros y sus extremos o telómeros) y permiten así determinar con mayor rapidez y precisión (respecto de las técnicas de citogenética clásica, como la tinción homogénea de los cromosomas con Giemsa o los bandeos cromosómicos) los reordenamientos cromosómicos (aberraciones) estructurales.
De este modo, en extendidos cromosómicos (portaobjetos de vidrio que contienen células con cromosomas en la etapa de la mitosis llamada metafase), identificamos con la ayuda de un microscopio de fluorescencia las diversas anomalías estructurales producidas por los mutágenos bajo estudio (cromosomas con más de un centrómero, cromosomas en forma de anillo, fragmentos cromosómicos, etc.). Luego, obtenemos la frecuencia de aberraciones o anomalías cromosómicas estructurales por célula y comparamos este dato con el obtenido a partir del análisis cromosómico de células normales, no expuestas al mutágeno.
“Evaluamos así el efecto clastogénico (daño cromosómico) del mutágeno en cuestión, determinando si el compuesto es o no mutagénico a nivel cromosómico, qué tipo de aberraciones produce y si existe relación entre la concentración (si es un mutágeno químico) o dosis (si es un mutágeno físico) utilizada del mutágeno y la frecuencia de aberraciones inducida por el mismo” explicó el científico de la UNLP.
También se estudian los posibles mecanismos mediante los cuales los mutágenos producen los efectos clastogénicos sobre los cromosomas, agregando diversas sustancias a los cultivos celulares que pueden modular dichos efectos. Esto permite evaluar la posibilidad de potenciar o inhibir los efectos de los mutágenos sobre los cromosomas.
Asimismo, se llevan a cabo estudios colaborativos con diversos grupos de investigación nacionales y extranjeros, que tienen por finalidad el estudio del daño cromosómico en células tumorales o expuestas a diversos mutágenos físicos y químicos.
Por otra parte, se han realizado y se continúan realizando con otros grupos de investigación estudios de localización y distribución de secuencias teloméricas en los cromosomas de diversas especies de la fauna de nuestro país (especies de ratones, monos, tortugas, armadillos, etc.), con el fin de ampliar la información citogenética existente acerca de dichas especies.
Además, el Dr. Bolzán colabora con el Sector de Cultivos Celulares del IMBICE (a cargo del Qco. Daniel Castrogiovanni, Profesional de Apoyo del CONICET y de la Lic. Julieta Parisi, Profesional de Apoyo de la CICPBA) en el dictado del curso de postgrado sobre cultivos celulares y sus aplicaciones (auspiciado por la Facultad de Ciencias Naturales y Museo de la UNLP), siendo uno de sus directores, y en la realización de ensayos de genotoxicidad de biomateriales (implantes dentales, válvulas cardíacas, etc.). Además del Dr. Bolzán y de la Lic. Cardozo, forman parte del grupo de investigación del Laboratorio de Citogenética y Mutagénesis, Mariana Ayala (pasante “ad-honorem”), Candela Fernández (pasante “ad-honorem”) y Ruth Sitkewich (concurrente “ad-honorem”), todas alumnas de la Facultad de Ciencias Naturales y Museo de la UNLP.